
原子发射光谱的基本原理是什么?
发布时间:2017-12-13 15:09 原子或离子受到热能、电能或光能等能量的作用时,外层电子得到一定能量后,由低能级E1跃迁至高能级芯E2这时的原子(或离子)是处于激发态,而给予原子(或离子)的能量(热能、电能或光能)即△E=E2——E1,称为激发能或激发电位,其单位以电子伏特eV表示。处于激发态的原子(或离子)其外层电子是不稳定的,它只能在高能态的轨道上停留约10-8 S,然后自发地跃迁到低能级轨道上,其能量以光的形式发射出来,形成一条谱线,其波长为:
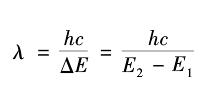
式中:
c——光速,等于3*108m/h
h——普朗克常数,其值为6.6262*10-34J.s
E1——低能级的电子能量
E2——高能级的电子能量
处于高能级的电子也可经过几个中间能级跃迁回到基态能级,这时可产生几种不同波长的光,在光谱中形成几条谱线,它们组成该元素的原子光谱。由于不同元素的电子结构不同,因而其原子光谱也不同,具有明显的特征。然而人们观察到的各个元素的所有谱线并不是在任何条件下都会同时出现,例如镉,当它的含量为1%时,有14条谱线出现;含量为0.1%时,有10条谱线出现;含量为0.01%时,有7条谱线出现;含量为0.001%时,仅有2条谱线出现,其波长分别为226.502nm和228.802nm,这两条谱线称为镉的线,又叫灵敏线。根据灵敏线的存在与否即可进行定性分析,判断试样中是否有该元素的存在。这些元素含量很低但仍然能够出现的光谱线,一般是共振线,或是激发电位的谱线,这样的谱线跃迁几率是的。当然,也有跃迁几率较大但不是共振线的。元素的灵敏线在许多分析书籍和手册上均可查到。
光谱定量分析的基础是光谱线强度与元素浓度的关系,通常利用罗马金和赛伯提出的经验公式:
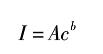
式中:
I——谱线强度
A——发射系数
c——元素含量
b——自吸系数
发射系数A与试样的蒸发、激发和发射的整个过程有关,还与光源类型、工作条件、试样组分、元素化合物形态以及谱线的自吸收现象有关,由激发电位和元素在光源中的浓度等因素决定。
元素含量很低时,谱线自吸收很小,这时b=1;元素含量较高时,谱线自吸收较大,这时b<1。I=Acb校正曲线,只有当b=1时才是直线,b<1时是曲线。当用罗马金公式的对数形式时,只要b是常数,就可得到线性的工作曲线。
发射光谱分析根据接受光谱辐射的方式不同,分为看谱法、摄谱法和光电法,看谱法是用眼睛直接接受谱线;摄谱法是用感光板接收谱线,然后经过显影定影等过程,在映谱仅或黑度计上读谱,主要仅器是摄谱仅;光电法则是用光电转换元件来接收光谱信号,主要仅器有光电直读光谱仅,电感耦合等离子体光谱仅。无论何种仅器,其主要构成部件均是光源、分光仅(棱镜和光栅)、检測器(感光板、光电倍增管、电感耦合器件和电荷注入器件等)。
免责声明: 凡注明来源本网的所有作品,均为本网合法拥有版权或有权使用的作品,欢迎转载,注明出处。非本网作品均来自互联网,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。