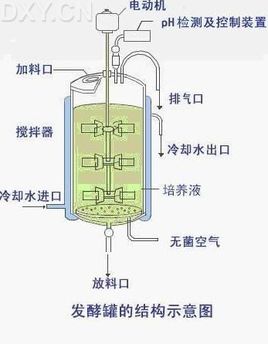
生物反应器
生物反应器(英语:Bioreactor)是指任何提供生物活性环境的制造或工程设备。在一种情况下,生物反应器是一个进行涉及到生物或生物化学活性物质由特定的生物生产出来的化学过程的容器。此过程既可以有氧进行也可以无氧进行。这些生物反应器通常呈圆筒状,其体积从几升到几立方米不等,常由不锈钢制成。
应用
.改良乳汁品质;
2.生产药用蛋白。
3.外源基因在动物体内的位点整合问题;
4.乳蛋白基因表达组织特异性问题;
5.目的蛋白的翻译后修饰问题;
6.转基因表达产物的分离和纯化问题;
7.转基因的技术与方法问题;
8.伦理道德问题。
膀胱生物反应器
膀胱反应器有着和乳腺反应器一样的优点:收集产物蛋白比较容易,不必对动物造成伤害。此外,该系统可从动物一出生就收集产物,不论动物的性别和是否正处于生殖期。膀胱生物反应器最显著的优势在于从尿中提取蛋白质比在乳汁中提取简便、高效。
膀胱生物反应器多用Uroplakin启动子启动人生长激素(hGH)的表达,产生 hGH特异性的高丰度RNA,这些RNA与蛋白分泌量高度相关。Uroplakin基因在多种哺乳动物体内有很高的保守性,如鼠、兔、牛、羊和人等。
生长激素 Kerr等[12]将pUPII-LacI用质粒的Kpn i进行消化,用T4DNA多聚酶切去3'端,然后用BamHI消化,分离出3.6kb的5'端小鼠UPII基因片段,此片段含有膀胱反应器特异性表达所需的大部分序列。将此片段与位于无启动子的pOGH质粒纯化SaI和BamHI位点间的hGH结构基因的5'端连接,得到pUPII-hGH质粒,能表达该质粒的组织分布有限。将得到的pUPII- hGH质粒用HindIII和EcoRI消化,得出一段5.7kb的UPII-hGH融合基因可用于显微注射,在膀胱上皮细胞中合成hGH,收集转基因动物尿液,从中提取重组蛋白。但在这一途径中转基因动物会因hGH的作用逐渐肥胖,并导致雌性动物不育症。乳腺生物反应器也能表达hGH。用同源重组方法将hGH基因导入210kb的人α-乳球蛋白位置依赖性YAC载体,将重组的YAC dNA显微注入大鼠胚胎,转基因大鼠的乳汁中含有高水平的hGH,含量可达0.25~8.9mg/ml[13]。
翻译与修饰
转基因动物分泌的蛋白,特别是糖链成分的结构与人体蛋白有差异。因此研究分泌蛋白的修饰就显得很重要。在乳腺生物反应器中,蛋白质翻译前修饰的主要方式是在多个位点对乳腺中的蛋白前体进行信号肽剪切和对糖链进行修饰。例如,从山羊乳液中得到的长效组织型纤溶酶原激活剂与人体内和相比较,含有少量的异种(外源)低聚糖,同时,唾液酸、N-乙酰葡萄糖胺和半乳糖含量明显减少,关且出现缺少蛋白质C127的N-乙酰半乳糖胺。此外,从猪乳液中得到的C蛋白中是没有的;从羊乳液中得到的重组α1-抗胰蛋白酶多聚肽也反映了唾液酸酸化程度的差异;在山羊乳腺中观察到了重组抗凝血酶Ⅲ上低聚甘露糖与特异天冬酰胺的位点特异性聚合等等。研究小鼠乳液中的重组γ-干扰素可对翻译前修饰有更好的理解,γ-干扰素有大量的位点特异性变化,在N端连接位点进行复杂的唾液酸酸化和连接核心岩藻多聚糖,其次是低聚甘露糖。与从小鼠细胞中取得的蛋白质相比,分泌的重组蛋白没有GalNAc、NeuGC和Gal∞l 、3Gal-βl、 4GlcNAc残基。这些蛋白特异性的糖基化类型可与细胞上的受体结合并清除病人体内的重组蛋白,因此可能会影响疗效,最终的结果尚有待验证。
同源组织表达蛋白质的优点是可对表达产物进行调控并校正珠蛋白链的翻译过程,避免无效的翻译前修饰,使产物蛋白尽可能与人体天然蛋白相似,降低人体内的排斥反应,提高药物蛋白疗效。目前,蛋白分离技术飞速发展,大大提高了蛋白质分离的可行性和分离效率。第二种技术路线中目前以乳腺生物反应器较为多见,因为乳汁易得到,且乳汁中的特异蛋白含量较大,对蛋白水解酶的降解作用也比较稳定。乳汁是一种混合物,含3%~6%的总蛋白,3%~5%的脂类,对蛋白提纯技术要求比较高。另一方面,药用蛋白是在动物乳腺中产生。因此只有含转基因型人雌性动物在泌乳期才能生产药用蛋白,可用的动物数目有限,且生产期较短。膀胱生物反应器的优点在于含有转基因型的两性动物都可用,产后收集时间长,提取产物蛋白浓度双乳液中的含量低得多,尽管收集的尿液多且时间长,生产单位数量的药用蛋白在乳腺和膀胱生物反应器中的成本是差不多的
问题与展望
在转基因动物生物反应器的应用中,有些问题尚待解决。比如,由于转基因动物的基因是镶嵌整合型的,因此它的下一代并不都转基因型。但是在绵羊,猪和山羊中观察到只要转基因型从起始个体传给了下一代,这种转基因型就可以稳定地遗传好几代。而其他一些因素,如外源基因的整合率低,胚胎移植的受孕率低等都使有效的转基因动物大大减少。同时,由于对调控表达水平的程序,指导进行精确的组织特异性和发育调控表达的程序,以及调控和编码内含子序列间可能的相互作用的认识尚不充分[14],容易引起异位点表达;由于现在的技术还不能控制整合的位点,因此存在对内源基因进行插入诱变的可能性,转基因型的表达会受整合的不同位点的影响。这些因素使得在家畜长成前,要用小鼠对新基因构型进行常规试验。
转基因动物生产的药用蛋白可用于预防和治疗疾病,其转运系统及口服用药引起的耐受性等问题都在作进一步研究。以转基因家畜生产珍贵的药用蛋白具有重大的经济价值和社会效益,这项生物技术最终将会得到广泛应用。
优点
1.成本低
2.设备简单
3.效率高
4.产品作用效果显著
5.减少工业污染
乳腺生物
将所需目的基因构建入载体,加上适当的调控序列,转入动物胚胎细胞,使转基因动物分泌的乳汁中含有所需要药用蛋白。从融合基因转入胚胎细胞到收集蛋白质有一个过程,包括胚胎植入、分娩和转基因动物的生长。转基因动物从出生到次泌乳,猪、羊、牛各需12、14、16个月;并且只有雌性动物泌乳且不连续,一般可持续2、6、10个月。牛、羊等大型家畜能对药用蛋白进行正确的后加工,使之具有较高的生物活性,同时产奶量大,易于大规模生产,因而成为乳腺生物反应器理想的动物类型。
抗凝血酶Ⅲ
个进入临床试验的转基因蛋白产物是抗凝血酶Ⅲ,将半乳糖β-酪蛋白的启动子和含抗凝血酶Ⅲ基因序列相连,转入绵羊胚胎细胞,在转基因绵羊的乳液中得到有生物活性的蛋白产量可达7g/L[2]。目前该蛋白正用于冠状动脉旁路手术患者的二期临床验证。
β-乳球蛋白
在实验过程中人们发现牛的β-乳球蛋白(BLG)基因非常稳定,并能在乳腺中特异性表达。Hyttinen等[3]将含有5'端2.8kb和3'端1.9kb的牛BLG基因片段构建成载体,转入小鼠胚胎细胞,可在转基因小鼠的乳腺中特异表达高水平的BLG,此外,还发现CpG位点的甲基化程度与BLG的表达量有关,甲基化少的转基因小鼠乳液中BLG分泌量较大,可达1~2mg/ml,而其他转基因小鼠分泌量小于0.1mg/ml。
红细胞生成素
(EPO) 目前国内外均采用CHO细胞表达生产人EPO,成本比较昂贵,而用转基因动物生产的EPO,可能是一条理想的途径。将EPO dNA分别以HindⅢ和BamHI酶切,1%琼脂糖凝胶电泳回收5.4kb的HinⅢ/BamHI片段,插入pGEM-7zf(+)载体,再将867bp的BLG启动子插入EPO基因之前EcoR、ClaI位点,构建表达载体pGEM-3zf(+)β-LG-EPO。通过显微注射方法得到转基因小鼠乳汗中的EPO含量可达0.5μg/ml[4]。
生物反应器
生物反应器
α1-抗胰蛋白酶这也是一个利用BLG基因构建的重组蛋白。将BLG5'末端4.0kb序列与人的α1-抗胰蛋白酶(α1AT)基因的6.5kb片段(去掉个内含子)融合,再连接羊的BLG启动子,以pPOLYⅢ-Ⅰ为载体,转入羊的胚胎细胞,可在转基因羊分泌的乳液中得到含量高达60.0mg/ml的重组蛋白α1AT[5]。转基因在两年前进入了临床验证。
因子Ⅸ
Schnieke等[6]将羊的BLG基因5'末端和人的因子Ⅸ cDNA 与含有BLG复制单元和3'末端的片段融合,将构建的杂合基因转入羊的胚胎细胞,从分泌的乳汁中得到125μg/ml的重组蛋白。黄淑帧教授等[7]构建了一个含有小鼠MAR元件、牛β-酪蛋白基因调控序列和hFⅨ微基因的hFⅨ乳腺组织特异性表达载体pMCⅨm,其中hF Ⅸ微基因包括全长hF Ⅸ cDNA ,800bp经过改造的内含子1序列和hFⅨ蛋白的信号肽序列。将线形化的表达载体pMC Ⅸm导入羊的受精卵。转基因羊分泌的乳汁中hFⅨ蛋白的含量约为95ng/ml。在另一实验中,Yull等[8]将BLG5'末端序列,fⅨ编码序列和缺失隐性3'端连接点的f Ⅸ3'末端不翻译区域的一个小片段融合,构成杂合基因,去掉SphI和SmaI位点,克隆入移去了pBJ41的SphI/EcoRV。转入小鼠胚胎细胞,得到的重组蛋白产量达0.06mg/ml。经过进一步研究,发现是转基因动物乳腺中对DNA的错误剪切使分泌量降低,从而增高重组蛋白产率。在乳腺组织中表达有完全活性的因子Ⅸ是比较成功的,尤其是乳腺组织对因子Ⅸ N端附近的一段含12个葡萄糖残基的序列进行γ-羧化以保持其活性,而在以前的天然蛋白中没有发现γ-羧化作用。
因子Ⅷ
人FⅧcDNA长约7.2kb,是目前为止表达的最长cDNA。将它插入小鼠的乳清酸性蛋白(WAP)基因中启动子(2.5kb)的下游,使之在乳腺中靶向分泌FⅧ重组蛋白。在WAP/FⅧcDNA构建的转基因小鼠中rFⅧ表达,而在转基因猪中可达1.0~2.7μg/ml[9]。
单克降抗体
Castilla等[10]将编码了重组单克降抗体(rMab)6A.C3的免疫球蛋白基因cDNA插入小鼠WAP dNA基因组的个外显子,使rMab 6A.C3的表达可以由WAP基因调控序列来控制,将构建的杂合基因注入小鼠胚胎细胞原核,使小鼠乳腺分泌有活性的单克降抗体,这种转基因表达产物将广泛应用于预防新生儿肠道感染。
C蛋白
同样在WAP基因的个外显子位点,Drews等[11]将人C蛋白cDNA插入,转入小鼠胚胎细胞,可得到产量达1.6mg/ml的重组蛋白。而将上述杂合基因转入猪的胚胎细胞,可使猪分泌出380μg/mlμg/ml·hr的外源蛋白,活性与人血浆中C蛋白的活性相同。由于C蛋白的抗凝活性依赖于轻链膜结合区域正确的γ-羧化,因此,转基因猪能分泌有活性的C蛋白表明猪的乳腺细胞可对C蛋白前体高速率地进行γ-羧化,以使成熟C蛋白有完整的活性。
生产蛋白
转基因动物表达重组蛋白多以乳腺、唾液腺和膀胱为靶位。在这些表达器官中,通过构建合适的载体,选择适当的启动子和调控序列可产生比正常水平高得多的重组蛋白。不过,生产系统应尽可能与循环系统隔离,以减少表达产物对宿主动物的影响。
同源组织
目前,在同源组织中表达蛋白质最典型的例子是在动物的红细胞中表达人的血红蛋白。在人的血红蛋白基因编码序列里启动子有2个CACCC盒,而对应的猪的启动子里只有一个,另一个靠近它的是CGCCC盒。Sharma等[1]将猪的β-启动子与人的β编码基因融合,并将人的β-基因座调控区(β-LCR)和α、ε基因与融合基因的β基因连接在一起构成载体,转入猪胚胎细胞,从转基因猪分泌乳汁中得到的重组人血红蛋白含量高达32g/L。
基因构建
《国外医学》预防、诊断、治疗用生物制品分册1999年第22卷第5期
关键词:转基因动物生物反应器 药物 基因构建 表达
摘要 近年来,生物学和分子生物学研究领域的成就促进了转基因动物生物反应器的蓬勃发展。用转基因动物生物反应器生产药用蛋白是生物技术领域里的又一次革命,它以一个全新生产珍贵药用蛋白的模式区别于传统药物的生产。本文着重介绍转基因动物生物反应器的基因构建以及转基因动物组织特异性表达的进展。
以合理的费用获取大量在人体内原本稀少的血浆蛋白在不久前还只是幻想。然而,近年来生物学和分子生物学取得的显著进展终于使这种幻想成为现实。其中,将外源DNA用显微技术注入生殖细胞的原核,将重组DNA转入小鼠胚胎细胞和将DNA整合入宿主染色体和种系传递等重要发现,使用转基因(Tg)动物生产药用蛋白成为可能。此外,生物学技术的发展,如对卵细胞的获得、操作以及再植入和重组DNA等技术进步都为转基因动物生物反应器的成功提供了保证。
转基因动物生物反应器生产药用蛋白一般有两种技术路线。种是将目的基因在同源组织中表达蛋白质;第二种是将目的基因构建成杂合基因,转入动物胚胎,通过转基因动物的分泌器官收集并提纯药用蛋白。转基因动物分泌的蛋白经过后加工酷如人体天然蛋白的结构,也有完全相似的生物活性。
输卵管
1993年英国罗斯林研究所Sang博士研究禽类蛋黄表达系统,在鸡蛋的蛋黄里表达了外源
蛋白质,由于蛋黄蛋白质是在肝脏细胞表达的蛋白质,而且含量不高;因此,1994年中国科学院微生物研究所、中国转基因动物学会(筹)副秘书长曾(杰)邦哲提出了禽类转基因输卵管生物反应器,在国际上最早开展采用蛋清蛋白质基因侧翼序列表达外源药用蛋白质的研究,1994年11月(Glodegg Plan)和1995年3月及1996年转基因动物通讯、1995年7月上海首届国际生物技术与药物学术研讨暨展览会、1996年11月北京第1届国际暨第3届全国转基因动物学术研讨会(秘书长曾邦哲)、1997年生物技术通报发表,并创造了“输卵管生物反应器(oviduct bioreactor)”一术语与词汇,以及1999年在德国创建的系统生物科学与工程网站阐述了输卵管生物反应器(oviduct bioreactor)概念、方法与技术研究。1996年创办第1届国际转基因学术研讨会期间,曾邦哲与加拿大、美国、英国、日本有关转基因禽类实验室联系,但国际上当时没有人开展这项课题,随后与美国Avigenics公司和Georgia大学R.Ivarie教授探讨了输卵管生物反应器的合作研究。1998年,美国Avigenics公司独立开展了规模化投资与研究开发输卵管生物反应器,因中国科学家曾邦哲已经去了以色列。2002年后,国际国内掀起了输卵管生物反应器的研究开发热潮,2003年Science发表了Gloden Egg的评述文章。目前,国际上已有十多家前景看好的公司以输卵管生物反应器作为拳头开发产品,约2003年英国罗斯林研究所也创建了公司,并由Sang博士主持研究课题,从禽类蛋黄表达系统转向了输卵管生物反应器。输卵管生物反应器将称为继哺乳动物乳腺生物反应器后发展前景的动物生物反应器。
概述
名称:生物反应器
主题词或关键词:DNA生命科学细菌胰岛素
生物反应器:生物反应器是利用生物体所具有的生物功能,在体外或体内通过生化反应或生物自身的代谢获得目标产物的装置系统、细胞、组织器官等等。
内容
生物反应器听起来有些陌生,基本原理却相当简单。胃就是人体内部加工食物的一个复杂生物反应器。食物在胃里经过各种酶的消化,变成我们能吸收的营养成分。生物工程上的生物反应器是在体外模拟生物体的功能,设计出来用于生产或检测各种化学品的反应装置。或者说,生物反应器是利用酶或生物体(如微生物)所具有的生物功能,在体外进行生化反应的装置系统,是一种生物功能模拟机,如发酵罐、固定化酶或固定化细胞反应器等。
在固定化酶广泛应用的基础上,人们发现天然细胞本身就具有多功能的系列化反应系统采用物理或化学方法将细胞固定化,是利用酶或酶系的一条捷径。一个固定化细胞反应器犹如一台“生命活动功能推动机”。固定化细胞技术开始于70年代,其实际应用程度已超过固定化酶。如美国、欧洲、日本均采用固定化菌体柱床工艺大规模生产高果糖浆。
简介
生物反应器是利用酶或生物体(如微生物)所具有的生物功能,在体外进行生化反应的装置系统,它是一种生物功能模拟机,如发酵罐、固定化酶或固定化细胞反应器等。在酒类、医药生产、浓缩果酱、果汁发酵、有机污染物降解方面有重要应用。
发展阶段
生物反应器(bioreactor)经历了三个发展阶段:细菌基因工程、细胞基因工程、转基因动物生物反应器。转基因动物生物反应器的出现之所以受到人们极大的关注,是因为它克服了前两者的缺陷,即细菌基因工程产物往往不具备生物活性,必须经过糖基化、羟基化等一系列修饰加工后才能成为有效的药物,而细胞基因工程又因为哺乳动物细胞的培养条件要求相当苛刻、成本太高而限制了规模生产。另外,转基因动物生物反应器还具有产品质量高、容易提纯的特点。一般把目的片段在器官或组织中表达的转基因动物叫做动物生物反应器。几乎任何有生命的器官、组织或其中一部分都可以经过人为驯化为生物反应器。从生产的角度考虑,生物反应器选择的组织或器官要方便产物的获得,例如乳腺、膀胱、血液等,由此发展了动物乳腺生物反应器、动物血液生物反应器和动物膀胱生物反应器等。其中,转基因动物乳腺生物反应器的研究最为引人注目。
转基因动物生物反应器
用微生物、植物、动物或人细胞,或者用专一性酶通过生物方法将原料转化为特定产品的容器称为生物反应器。通常微生物和细胞又涉如何维持它们的环境以提供的生长条件的问题。生物反应器能通过提供合适的条件:例如温度、pH、有效的底物、营养盐、维他命和氧(对好氧有机物)来支持这个自然过程,使细胞能进行生长和新陈代谢。生物反应器(bioreactor) 经历了3 个发展阶段细菌基因工程、细胞基因工程、转基因动物生物反应器。细胞基因工程产物往往不具备生物活性,必须经过糖基化、羟基化等一系列修饰加工后,才能成为有效的药物,而细胞基因工程又因为哺乳动物细胞的培养条件要求相当苛刻,成本太高,限制了规模生产。动物生物反应器具有产品质量高,容易提纯的特点,弥补了其它各类基因表达系统的缺陷。
转基因动物生物反应器
转基因动物是指经人的有意干涉,通过实验手段,将外源基因导入动物细胞中,稳
利用基因工程培育新型微生物
利用基因工程培育新型微生物
定地整合到动物基因组中,并能遗传给子代的动物。Palmiter等(1982)将含有小鼠金属巯蛋白基因启动子的DNA片断与大鼠生长激素基因融合,用微注射的方法导入小鼠受精卵,移植给受体,产下了21 只仔鼠,6 只比同窝仔鼠生长快,10周龄时体重比同窝正常鼠大1 倍,成功地获得了超级小鼠。这一结果引起世界轰动,转基因动物的内在潜力由此而得以证实。随后世界各国普遍开展了转基因动物的研究,目前已有转基因小鼠、猪、牛、鱼、鸡等多种转基因动物问世[1]。转基因动物的主要技术步骤包括目的基因的分离与克隆;表达载体的构建;受体细胞的获得;基因导入;受体动物的选择及转基因胚胎的移植;转基因整合表达的检测;转基因动物的性能观测及转基因表达产物的分离与纯化;转基因动物的遗传性能研究以及性能选育;组建转基因动物新类群
等。转基因动物最为诱人的前景是利用它生产人类所需要的生物活性产品或药物。目前世界上有很多公司正在致力于这方面的研究。而转基因家畜研究最为活跃的领域就是利用它们生产新的动物产品。通常把目的基因在血液循环系统或乳腺中表达的转基因动物称为动物生物反应器,把家畜作为一种生物反映器,生产人类所需的药用蛋白,包括治疗用药物、激素和抗体等。
动物血液生物反应器
近年来,动物血液生物反应器取得了很大进展。血液生物反应器比较适合生产人血红蛋白、抗体和生产非生物学活性状态的融合蛋白,而有活性的蛋白或多肽(如激素、细胞分裂素、组织血纤维溶酶因子等)由于进入了动物血液循环系统而影响动物的健康。到目前为止,已有多种通过转基因动物生产的具有生物学功能的人血红蛋白问世。
动物的乳腺生物反应器
乳腺生物反应器的原理是外源基因在乳腺特异性表达需要乳蛋白基因的一个启动子和调控区,即引导泌乳蛋白基因表达的序列,将外源基因置于乳腺特异性调节序列之下,使之在乳腺中表达,通过回收乳汁获得重要价值的生物活性蛋白。从目前的研究成果看,与传统的原核系统及细胞发酵系统相比,动物乳腺生产的重组蛋白产品具有以下特点:生物活性高,无污染,纯化简单,产量高,成本低。目前,已克隆并用作构建载体的乳蛋白基因主要有-乳球蛋白(BLG)基因、s1-酪蛋白基因、-酪蛋白基因、乳清酸蛋白(WAP)以及乳清蛋白基因[2]。大多数的乳蛋白基因的启动子已用于外源基因在转基因动物乳腺中的表达。s1-酪蛋白基因和-乳球蛋白的启动子尚有未知因素的作用,它们在转基因动物中表达水平低或表达不稳定。-酪蛋白的启动子在转基因动物中表达水平也很低。绵羊-乳球蛋白、山羊酪蛋白和牛s1-酪蛋白启动子在转基因动物乳腺中维持异种蛋白的表达水平较高。如果得用目的基因的DNA序列而不是cDNA,表达效果可能会更好。不翻译的外显子和内含子的掺入可能有利于
转基因的表达。值得一提的是,利用乳腺生物反应器生产的“新奇牛奶”已经问世。2003 年,Brophy 等通过共转染和嘌呤霉素筛选向牛胎儿成纤维细胞引入-s蛋白基因和-酪蛋白基因的多量拷贝,而后进行核移植生产出了8 头转基因奶牛,其产奶中酪蛋白总量较普通奶高30%。这种奶的蛋白和钙含量提高,热稳定性增强而乳糜颗粒变小,其营养价值更高,也更适于奶酪生产[3]。
优越性
转基因动物的问世,为利用基因工程手段获得低成本、高活性和高表达的产物开辟了一条重要途径。作为生物反应器的转基因动物,主要是利用其乳腺组织和血液组织进行定位表达,特别是用乳腺组织生产具有生物活性的多肽药物和具有特殊营养意义的蛋白质,已成为一个新兴的转基因制药业,它的优越性有如下几点[4]。3.1 表达产物能充分修饰且具有稳定的生物活性 利用DNA重组技术的微生物发酵工程来生产的药用蛋白,由于细菌等微生物不能进行蛋白质合成后的加工,因而生物活性低,并且具有免疫原性,而利用转基因动物生产药用蛋白却免除这些问题。
成本低可以大规模生产
作为生物反应器的转基因动物可无限扩繁,且饲养成本低,可进行大规模的药物生产。而动物细胞生物反应器,虽然能生产具有完全生物活性的产品,但以商业生产为目的的大规模的动物细胞培养,成本会极高且培养条件要求苛刻。
产品质量高易提纯
由动物生物反应器生产的药品为纯的生物制品,避免了化学试剂及生物毒素的污染。目前,某些药用蛋白生产已达每千克乳汁含几十克,生物活性与天然蛋白几乎完全一样,极易提纯。总之,动物生物反应器弥补了其它各类基因表达系统的缺陷。
应用
以动物的乳腺或其它组织作为生物反应器生产贵重的医用蛋白,是动物转基因技术的另一特殊形式。由于转基因动物的遗传结构发生了变化,并能稳定地遗传给后代,外源基因不仅能在转基因动物得到整合和表达,而且能获得组织特异性(乳腺组织)和发育特性(妊娠后期和泌乳期)表达,利用这一点能产生转基因泌乳家畜,还能生产出目前短缺而又十分珍贵的医用蛋白。近十年,这方面的研究在英、美、法、瑞士和荷兰等国家已相继展开,并取得了一定进展。截至目前,世界一些国家的生物技术企业在利用转基因动物作生物反应器研究开发的转基因动物药品有以下几种。
组织纤溶酶原激活剂(TPA):由美国遗传技术公司(Genentech) 用基因重组技术开发的血栓溶解剂,1987 年11 月经联邦食品及药物管理局(FDA)批准上市。1988 年的销售额为1.5 ~ 1.6 亿美元,1989年为1.8 ~ 1.9 亿美元。今后每年的市场销售额约为2 ~ 2.5 亿美元。
乳铁蛋白(lactoferrin): 用转基因奶牛生产。由于以转基因奶牛生产乳铁蛋具备产量高、成本低,以及有无限量增殖生化反应器等特征,因而备受各国瞩目。乳铁蛋白是一种口服的活性蛋白,自然产生于人乳中,它具有抗菌、传递铁素等特性。
人类-1 抗胰蛋白酶(AAT):-1 抗胰蛋白酶(AAT)缺乏是最常见的遗传代谢病,能引起肺和肝的损伤。-1 抗胰蛋白酶(AAT)为呼吸系统的非特异性可溶因子,它可抑制多种酶的活性,包括细菌的酶,以及中性白细胞溶酶体分泌的蛋白质、弹性蛋白酶、胶原酶、纤维蛋白溶酶和凝血酶。这项产品是从英国农业和食品研究委员会的动物生理和遗传研究院(IAPGR)研究成果为基础,近年由英国PPL 公司与德国拜耳公司共同尝试用转基因绵羊的羊奶生产AAT。
促红细胞生成素(EPO):以转基因猪生产。这种药物存于转基因猪的血液中。目前转基因猪血球素合成的遗传控制机制已十分清楚,用基因重组技术合成的EPO 已在多个国家上市。
重组人抗凝血酶ii(i atryn):世界上个动物乳腺生物反映器重组蛋白药物。Atryn的主要成分-重组人抗凝血酶iii 具有抑制血液中凝血酶活性,预防和治疗急慢性血栓血塞形成,对治疗抗凝血酶缺失症有显著效果。拒美国权威机构预测,到2010年,转基因动物生产的重组蛋白产品销售额将达到350 亿美元,生产的药物将占整个基因工程药物种类的90%以上。
存在的问题与发展前景
转基因动物与生物反应器是20 世纪生命科学发展的一个里程碑,但现在仍然存在着许多急需解决的问题。由于转基因动物的研究在理论和技术上尚有不完善之处,使得转入的外源基因在动物基因组中随机整合、调节失控、遗传不稳定,表达率不高。要提高转基因的效率,保证外源基因的有效表达,关键是基因构建的定点整合。转基因动物生物反应器的产品的安全性问题。这包括转基因动物的产物的分离和提纯,表达产物的结构和生物活性与人体蛋白的相似性的问题。只有从表达产物除去能引起人类变态反应的非人类蛋白,并且产品与人体蛋白有足够的相似性,才能应用于人类的健康事业。转基因动物的成活率低,出生后的部分个体表现出各种生理和免疫缺陷。如为提高生产性能而制备的转基因猪出现了雌性不育、胃溃疡和关节炎等病症; 而克隆牛已经先后死去; 转基因后获得的目的性状,通过有性繁殖后,遗传性状出现分离,如英国的一只高产1-AT 羊奶的转基因绵羊,其子代羊奶中的含仅为其母亲的1/10[6]。尽管转基因动物生物反应器的研究仍面临着许多需要解决的问题,但它
潜在的社会价值是无可估量的。在未来几年内,将有多种动物乳腺生物反映器重组蛋白上市,从而形成市场前景广阔和利润巨大的新生物制药行业。
参考文献:
[1]陈学进,曾申明,李和平.动物生物反应器[J].国外畜牧科技,1998,25⑴:39–43.
[2]袁建民,胡建宏,李青旺,等.动物乳腺生物反映器研究进展[J].中国农学通报,2006,3:20–25.
[3]张忠诚.动物乳腺生物反映器的原理及研究进展[J].中国奶牛,2006,4:9–12.
[4]邱磊,郭葆玉.转基因动物反映器的基因构建与表达[J].国外医学,1999,22⑸:41–44.
[5]孙博兴,侯万文,欧阳红生.转基因动物生物反应器[J].动物科学与动物医学,2000,3:18–20.
[6]林莉,胡佐忠.转基因动物研究进展[J].畜禽业,2005,5:19–23.
工程
生物反应器是使生物反应得以实现的装置。生物反应器有各种各样的形式,要使生物反应器运行得好,必须首先对生物反应器和反应特征有深刻的理解,这就是生物反应器工程的概念。生物反应器工程着重研究生物反应器本身的特性,如其结构和操作方式、操作条件对细胞形态、生长、产物形成的关系。它与生物反应工程结合,共同解决各种生物反应的生物反应器、操作条件的选择问题。